Titrace je metoda odměrné kvantitativní analýzy, tzn. slouží ke stanovení množství analytu. Je založena na přesném odměřování objemů pomocí pipet, byret a odměrných baněk.
Podle druhu probíhající reakce rozlišujeme titrace:
- Neutralizační (acidobazická)
- Srážecí
- Chelatometrické (komplexometrické)
- Redoxní (oxidačně-redukční)
Praktické provedení titrace
Během titrace zpravidla přidáváme k neznámému vzorku odměrný roztok o přesně známé koncentraci. Vždy je nutné zvolit vhodné činidlo. Reakce, která během titrace probíhá nesmí být rovnovážná a bod ekvivalence (tzn. bod, kdy je všechen vzorek ztitrován) musí být snadno detekovatelný.
Příprava roztoku o přesné molární koncentraci
Bližší informace o molární koncentraci najdete zde.
Molární koncentrace je dána hmotností (látkovým množstvím) rozpouštěné látky a objemem konečného roztoku. Pro přípravu roztoku o přesné koncentraci se používají odměrné baňky, které mají objem vyznačený ryskou na hrdle.
Přesně naváženou látku kvantitativně (beze ztrát) přesypeme do baňky. Přidáme vodu (ne do plna) a třepáním rozpustíme veškerou látku. Potom opatrně doplníme hladinu po rysku, pozor na meniskus, musí se dotýkat rysky spodním okrajem.
Dorovnávání hladiny na rysku je vhodné dělat kapátkem nebo pipetou. Pokud přidáte moc, tzn. pokud hladina vyleze nad rysku, je nutné začít od začátku.
Titrace
Titraci provádíme nejčastěji v titrační baňce, ale je možné využít i Erlenmayerovu baňku.


Do titrační baňky odpipetujeme roztok vzorku z odměrné baňky, stěny opláchneme vodou a přidáme indikátor (pokud je potřeba). Z byrety poté za stálého míchání přidáváme roztok činidla až do bodu ekvivalence.


Po dosažení bodu ekvivalence (zpravidla je indikován barevnou změnou) odečteme co nejpřesněji objem spotřebovaného roztoku činidla a vypočítáme koncentraci.
Indikátory
Jako indikátory slouží látky, která v blízkosti bodu ekvivalence mění svou barvu. Pro detekci bodu ekvivalence je možné použít i instrumentální metody, např. potenciometrii nebo pH-metrii.
Acidobazické indikátory
Jejich barva závisí na pH, vhodný indikátor musí mít barevný přechod v oblasti pH, kde se nachází inflexní bod titrační křivky.
| Indikátor | pH přechodu | Barevný přechod |
| Krystalová violeť | 0,0-2,0 | zelená-modrá |
| Kresová červeň | 0,2-1,8 | červená-žlutá |
| Dimethylová žluť | 2,9-4,1 | červená-žlutá |
| Bromfenolová modř | 3,0-4,6 | žlutá-modrá |
| Methyloranž | 3,1-4,4 | červená-žlutá |
| Methylčerveň | 4,4-6,2 | červená-žlutá |
| Bromthymolová modř | 6,0-7,6 | žlutá-modrá |
| Fenolftalein | 8,2-10,0 | bezbarvý-červenofialový |
| Tropeolin O | 11,1-12,7 | žlutá-hnědá |
Srážecí indikátory
Srážecí indikátory jsou závislé na typu použité reakce, u argentometrie se nejčastěji používá chroman draselný, který vytváří červenohnědou sraženinu chromanu stříbrného, ta má nižší hodnotu součinu rozpustnosti než AgCl a proto se sráží, až po spotřebování analytu, nejčastěji chloridů.
K2CrO4 + 2 AgNO3 → Ag2CrO4 + 2 KNO3

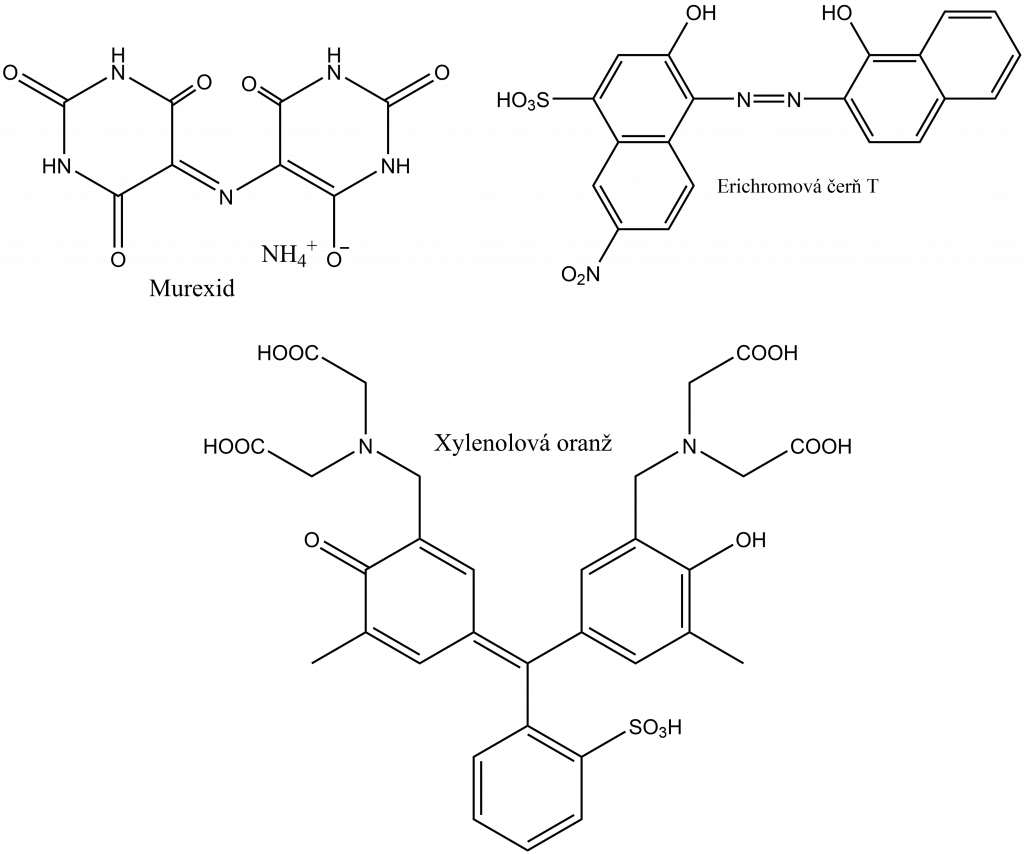
Indikátory používané u chelatomerie
Používají se metalochromní indikátory, ty tvoří barevné komplexy se stanovovanými kovy. Zpravidla jsou barevné, proto je přechod málo výrazný.
Výpočet
Pro výpočet titrace je nezbytně nutné mít k dispozici správnou a vyčíslenou chemickou rovnici děje, probíhajícího během titrace. Výpočet je velmi podobný klasickému stechiometrickému výpočtu.
Další ukázky výpočtů titrací najdete zde.
Jako příklad si můžeme uvést titraci hydroxidu sodného pomocí kyseliny chlorovodíkové. Navážku hydroxidu sodného (0,4525 g) jsme rozpustili ve 100 cm3 odměrné baňce. Na titraci jsme pipetovali třikrát 20 cm3. Odměrný roztok HCl měl koncentraci 0,1 M a faktor f=1,0583. Průměrná spotřeba kyseliny byla 18,55 cm3.
Rovnice titrace je jednoduchá, jde o klasickou neutralizační reakci:
NaOH + HCl → NaCl + H2O
Jak je vidět z rovnice jeden mol hydroxidu reaguje s jedním molem kyseliny, takže můžeme napsat:
$$\textrm{n(NaOH) = n(HCl)}$$
Pro výpočet potřebujeme také znát přesnou koncentraci kyseliny, ta se zpravidla uvádí přibližně (v našem případě 0,1 M) a zpřesňuje se faktorem. Přesnou hodnotu pak získáme vynásobením obou čísel.
$$\textrm{c} = 0,1 . 1,0583 = 0,1058\ \textrm{M}$$
Pro látkové množství pak platí vztah:
$$\textrm{n(NaOH) = c . V}\ =\ 0,1058\ .\ 0,01855\ =\ 0,00196\ \textrm{mol}$$
Toto vypočítané látkové množství odpovídá látkovému množství NaOH v 20 cm3 roztoku (k titraci jsme pipetovali právě tento objem). Abychom získali látkové množství v celé navážce, musíme ho vynásobit zřeďovacím faktorem:
$$\textrm{f}_\textrm{z}\ =\ \frac{\textrm{V}_{\textrm{celk}}}{\textrm{V}_{\textrm{pipet}}}\ =\ \frac{100}{20} = 5 \\
\textrm{n(NaOH) = c . V . f}_\textrm{z}\ =\ 0,1058\ .\ 0,01855\ .\ 5\ =\ 0,00981\ \textrm{mol}$$
Hmotnost hydroxidu v navážce pak vypočítáme snadno pomocí molární hmotnosti:
$$\textrm{m = n . M = }0,00981\ .\ 40\ =\ 0,393\ \textrm{g}$$
Celý tento výpočet můžeme provést najednou:
$$\textrm{m(NaOH) = c . f. V . f}_\textrm{z} . \textrm{M = }0,1\ .\ 1,0583\ .\ 0,01855\ .\ 5\ .\ 40\ =\ 0,393\ \textrm{g}$$
Čistotu hydroxidu sodného potom vypočítáme pomocí hmotnostního zlomku:
$$\textrm{w = }\frac{\textrm{m(NaOH)}}{\textrm{m(nav)}}\ =\ \frac{0,3926}{0,4525}\ =\ 0,868\ \Rightarrow 86,8\ \%$$
Pokud budeme titrovat hydroxid sodný kyselinou sírovou je nutné vzít v úvahu odlišný stechiometrický poměr reaktantů.
$$2\ \textrm{NaOH + H}_2\textrm{SO}_4 \rightarrow \textrm{Na}_2\textrm{SO}_4 + 2\ \textrm{H}_2\textrm{O} \\
\frac{\textrm{n(NaOH)}}{2} = \frac{\textrm{n(H}_2\textrm{SO}_4)}{1} \\
\textrm{n(NaOH) = 2 . n(H}_2\textrm{SO}_4) \\
\textrm{m(NaOH) = 2 . c . f. V . f}_\textrm{z . M}$$
Další kapitoly
- České chemické názvosloví
- Platné číslice a měření
- Základní chemické zákony
- Důležité veličiny a vztahy v chemii
- Výpočet stechiometrického vzorce
- Chemické rovnice a stechiometrické výpočty
- Koncentrace roztoků
- Rozpustnost, součin rozpustnosti
- Stavba atomu
- Periodická tabulka prvků a periodicita vlastností
- Chemická vazba
- VSEPR
- Komplexní sloučeniny
- Magnetické vlastnosti látek
- Termodynamika
- Chemická rovnováha
- Skupenské stavy látek
- Fázové rovnováhy
- Teorie kyselin a zásad
- pH, aktivita roztoku
- Elektrochemie
- Symetrie molekul
- Laboratorní technika
- Lineární regrese
- Jednotky tlaku
- Jednotky teploty
- Mohsova stupnice tvrdosti minerálů
- Odkazy
- Prezentace k semináři z obecné chemie
