Osmium je drahý kov, ve svých sloučeninách dosahuje oxidačního čísla v rozmezí -II až VIII. Společně s iridiem a platinou patři do triády těžkých platinových kovů.
| Atomové číslo | 76 | Počet stabilních izotopů | 5 |
| Atomová hmotnost | 190,23 | Elektronová konfigurace | [Xe] 4f14 5d6 6s2 |
| Teplota tání [°C] | 3033 | Teplota varu [°C] | 5012 |
| Elektronegativita | 2,2 | Hustota [g.cm-3] | 22,59 |
Izotopy
Osmium má sedm přírodních izotopů, z nichž pět je stabilních.
| Izotop | Zastoupení v přírodě [%] | Poločas rozpadu |
|---|---|---|
| 184Os | 0,02 | 3,0×1013 let |
| 186Os | 1,59 | 2,0×1015 let |
| 187Os | 1,96 | stabilní |
| 188Os | 13,24 | stabilní |
| 189Os | 16,15 | stabilní |
| 190Os | 26,26 | stabilní |
| 191Os | 40,78 | stabilní |
Známe cca 30 umělých radioizotopů osmia,[4] nejdelší poločas rozpadu má 194Os s poločasem rozpadu šest let.[5]
191Os
Tento izotop lze využít k přípravě jaderného izomeru 191mIr pro nukleární medicínu.[6]
$$^{191}_{\ \ 76}\textrm{Os}\ \rightarrow\ ^{191m}_{\ \ \ \ \ 77}\textrm{Ir}\ +\ ^{\ \ \ 0}_{-1}\beta$$
Výskyt a využití
V přírodě doprovází platinové kovy, patří mezi nejtěžší prvky. Vzácně se v přírodě vyskytuje jako osmiridium, což je slitina osmia s iridiem a často obsahuje i další platinové kovy. V lučavce královské se rozpouští pouze v jemně práškovém stavu.

Využití nachází ve slitinách s vysokou tvrdostí (např. s iridiem v osmiridiu) a jako součást heterogenních katalyzátorů.
Chemické vlastnosti
Je chemicky značně odolné, do roztoku jej lze převést alkalickým tavením s hydroxidem nebo peroxidem sodným. Jemné práškové osmium se na vzduchu samovolně oxiduje na oxid osmičelý.
Oxidy
Oxid osmičelý (OsO4) má tetraedrickou geometrii ale poměrně ochotně vytváří komplexní ionty, kde má osmium koordinační číslo 6. Je bezbarvý, ale často má nažloutlou barvu, což je způsobeno přítomností malého množství oxidu osmičitého. Vzniká přímou oxidací kovového osmia vzduchem.

Je to Lewisova kyselina a mírné oxidační činidlo, alkeny dokáže oxidovat na cis-dioly.
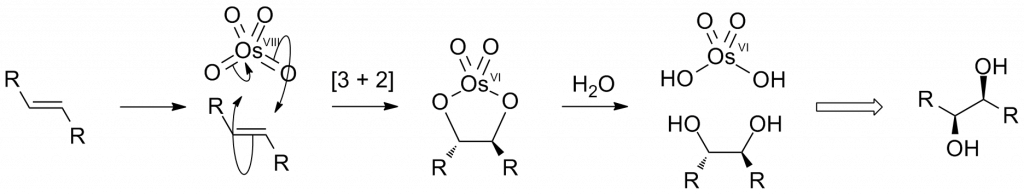
S vodnými roztoky reaguje za vzniku komplexních aniontů [OsO4(OH)2]2-, které lze snadno redukovat na [OsO2(OH)4]2-.
Reakcí amoniaku, OsO4 a KOH vzniká trioxonitridoosmičelan draselný, K[Os(N)O3].
Oxid osmičitý (OsO2) je hnědočerná krystalická látka, nerozpustná ve vodě, ale rozpustná v kyselině chlorovodíkové. Lze jej připravit oxidací osmia mírnými oxidačními činidly, např. chlorečnanem sodným nebo oxidem osmičelým.
Os + OsO4 → 2 OsO2
Karbonyly
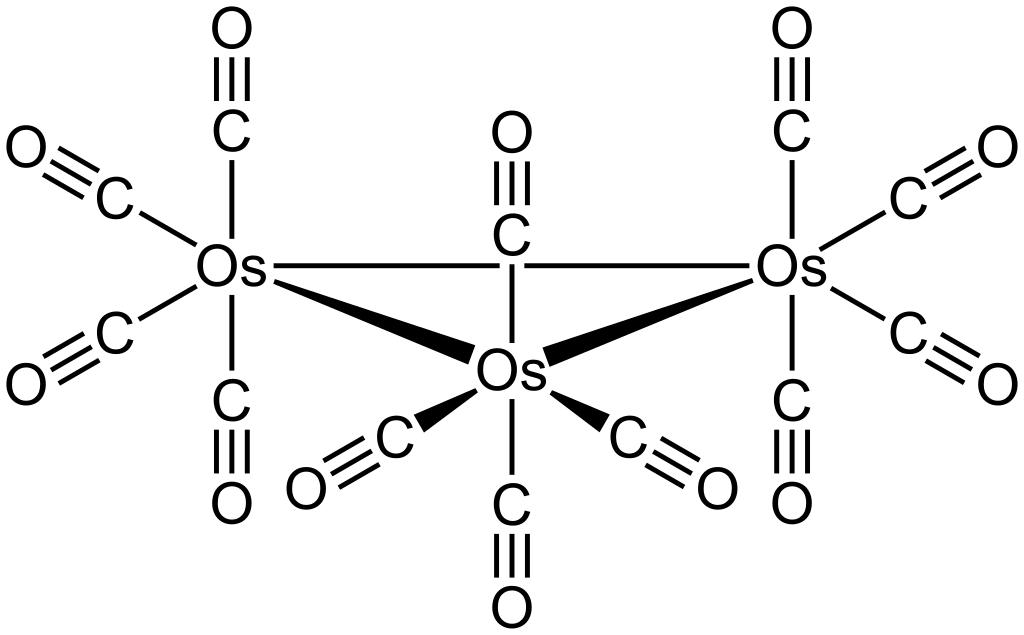
Reakcí oxidu osmičelého s oxidem uhelnatým za zvýšené teploty a tlaku vzniká triosmium dodekakarbonyl.
3 OsO4 + 24 CO → Os3(CO)12 + 12 CO2
Analog ferrocenu bez uhlíku
V roce 2026 byla připravena sloučenina [Os(η5-B5H10)2], kterou lze klasifikovat jako analog ferrocenu, který neobsahuje žádný uhlík.[7] Místo cyklopentadienylových ligandů (jako u ferrocenu) obsahuje borový analog těchto ligandů (B5H10).
NMR
Osmium má dva NMR aktivní izotopy 187Os a 189Os. Standardem pro Os NMR je OsO4.
Díky spinu ½ má 187Os užší signály než 189Os NMR, ale má podstatně nižší citlivost. Při měření se nejčastěji využívá nepřímé detekce.
Jádro 189Os má kvadrupól, z toho důvodu poskytuje široké signály. Toto jádro se měří lépe na spektrometrech s nižším polem.
| 187Os | 189Os | |
|---|---|---|
| Spin | 1/2 | 3/2 |
| Zastoupení v přírodě | 1,96 % | 16,15 % |
| Jaderný magnetický moment μ/μN | +0,06465189 | +0,659933 |
| Rozsah chemických posunů | -5000 až 0 ppm | |
| Relativní citlivost k 1H | 2,43×10-7 | 3,95×10-4 |
| Relativní citlivost k 13C | 1,43×10-3 | 2,32 |
Chemické posuny
| OsO4 | 0 | Klastry osmia | -2200-(-2800) |
| CpOs(phosphine)2Br | -3000-(-3500) | CpOs(phosphine)2Alk(en)yl | -4500-(-4900) |
Odkazy
- Osmium na české wikipedii
- Osmium na anglické wikipedii
- Osmium NMR
- Isotopes of osmium
- 194Os
- 191Os/191mIr-generator for studying arterial blood flow in experimental animal models
- [Os(η5-B5H10)2]: A carbon-free analog of ferrocene
Články o osmiu
- The Chemistry of Aromatic Osmacycles
- Determination of .delta.(187Os), J(Os,X), and T1(187Os) in osmium complexes via indirect 2D NMR spectroscopy
Navigace
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 |
| H | He | ||||||||||||||||
| Li | Be | B | C | N | O | F | Ne | ||||||||||
| Na | Mg | Al | Si | P | S | Cl | Ar | ||||||||||
| K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr |
| Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe |
| Cs | Ba | La | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn |
| Fr | Ra | Ac | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og |
| Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu |
| Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr |
4 Replies to “Osmium”