Sbírka řešených příkladů ke článku pH, aktivita roztoku.
Jaké je pH kyseliny chlorovodíkové o koncentraci 0,253 M?
Ukaž řešeníKyselina chlorovodíková je jednosytná silná kyselina, tzn,. že koncentrace protonů vzniklých disociací bude stejná, jako výchozí koncentrace kyseliny:
pH = -log c = -log 0,253 = 0,60
Skryj řešeníJaké je pH kyseliny sírové o koncentraci 0,253 M?
Ukaž řešeníKyselina sírová je silná, dvojsytná kyselina. Její disociací získáme dvojnásobnou koncentraci iontů H+.
H2SO4 → 2 H+ + SO42-
pH = – log c = -log 2*0,253 = -log 0,506 = 0,30
Skryj řešeníJaké je pH kyseliny octové o koncentraci 0,05 M?
Ukaž řešeníKyselina octová, CH3COOH, je slabá jednosytná kyselina, její disociační konstanta je pKa = 4,76. Koncentrace vodíkových kationtů je dána koncentrací kyseliny a její disociační konstantou.
$$pH = \frac{1}{2}pK_A – \frac{1}{2}\log\ c = \frac{1}{2} 4,76 – \frac{1}{2}\log\ 0,05 = 3,03$$
Skryj řešeníJaké bude pH roztoku anilinu o koncentraci 0,0258 M? pKb = 9,38
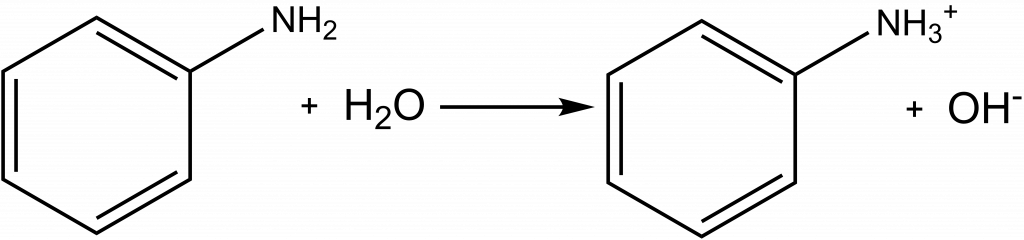
Anilin je slabá zásada, to je vidět už z uvedené pKb konstanty, proto použijeme vztah pro pH slabé zásady:
$$pH = 14 – \frac{1}{2} (pK_b – \log c) = 14 – \frac{1}{2} (9,38 – \log 0,0258) = 8,52$$
Skryj řešení100 cm3 roztoku NaOH o koncentraci 0,1035 M bylo napipetováno do 250 cm3 odměrné baňky a ta byla doplněna po rysku. Jaké je pH vzniklého roztoku?
Ukaž řešeníNejprve musíme vypočítat koncentraci NaOH po zředění. Prvním krokem bude výpočet látkového množství:
n = c . V = 0,1035 . 0,1 = 0,01035 mol NaOH
Koncentrace NaOH ve 250 cm3 odměrné baňce bude:
$$c = \frac{n}{V} = \frac{0,01035}{0,25} = 0,0414\ M$$
pH pak vypočítáme pomocí základního vzorce:
pH = 14 + log c = 14 + log 0,0414 = 12,62
Skryj řešení100 cm3 NaOH o koncentraci 0,5 M bylo smícháno se 100 cm3 kyseliny sírové o koncentraci 0,2 M. Jaká je koncentrace a pH vzniklého roztoku? Pro jednoduchost neuvažujme objemové změny.
Ukaž řešeníHydroxid sodný reaguje s kyselinou sírovou podle rovnice:
2 NaOH + H2SO4 → Na2SO4 + 2 H2O
Jde o neutralizační reakci, čili formálně reakci H+ s OH–. Proto potřebujeme spočítat látkové množství obou iontů:
n(OH–) = c . V = 0,5 . 0,1 = 0,05 mol OH–
Kyselina sírová je dvojsytná, proto poskytne dvojnásobnou koncentraci H+:
n(H+) = c . V = 2 . 0,2 . 0,1 = 0,04 mol H+
Ionty OH- jsou v nadbytku, po neutralizaci nám zůstane 0,01 mol iontů OH–. Pro výpočet pH potřebujeme znát jejich koncentraci:
$$c = \frac{n}{V} = \frac{0,01}{0,2} = 0,05 M$$
S pomocí koncentrace můžeme snadno vypočítat pOH a pak pH:
pOH = -log c = -log 0,05 = 1,3
pH = 14 – pOH = 14 – 1,3 = 12,7
Jaká je koncentrace kyseliny sírové o pH = 1,35?
Ukaž řešeníKyselina sírová je silná, dvojsytná kyselina. Její disociaci lze popsat rovnicí:
$$H_2SO_4 \rightarrow 2 H^+ + SO_4^{2-}$$
Koncentraci protonů vypočítáme ze vztahu pro pH:
$$pH = -\log [H^+] \\
c_{H^+} = 10^{-pH} = 10^{-1,35} = 0,045 M$$
Koncentrace kyseliny je rovna polovině koncentrace protonů, protože se z jedné molekuly kyseliny uvolní dva protony:
c = 0,023 mol.dm-3
Skryj řešeníJaká je molární koncentrace kyseliny fluorovodíkové o pH = 1,5?
Ukaž řešeníKyselina fluorovodíková, HF, je slabá kyselina. Její disociační konstanta je pKa = 3,15. Disociaci tedy můžeme popsat rovnovážnou reakcí:
$$HF \rightleftharpoons H^+ + F^-$$
pH je dáno mírně komplikovanějším vztahem, než pro silné kyseliny:
$$pH = \frac{1}{2}pK_a – \frac{1}{2} \log\ c \\
1,5 = \frac{1}{2}.3,15 – \frac{1}{2} \log\ c \\
-0,075 = – \frac{1}{2} \log\ c \\
\log\ c = 0,15 \\
c = 10^{0,15} = 1,41\ M\ HF$$
Kyselina fluorovodíková má koncentraci 1,41 mol.dm-3.
Skryj řešeníKe 100 cm3 roztoku NaOH o koncentraci 0,05 M bylo přidáno 20 cm3 roztoku HCl o koncentraci 0,1 M. Jaké bude pH výsledného roztoku? Objemové změny zanedbejte.
Ukaž řešenípH původního roztoku vypočítáme snadno, NaOH je silný hydroxid a je v roztoku zcela disociovaný.
$$pOH = -\log c = -\log 0,05 = 1,30 \\
pH = 14 – pOH = 14 – 1,30 = 12,70$$
Po přidání HCl proběhne neutralizační reakce a část NaOH zreaguje za vzniku NaCl:
NaOH + HCl → NaCl + H2O
Z rovnice vidíme, že reakce probíhá v poměru 1:1, tzn. jedna molekula NaOH reaguje s jednou molekulou HCl. Můžeme tedy snadno spočítat, kolik NaOH nám zůstane nezreagováno.
$$n(NaOH) = c . V = 0,1 . 0,05 = 0,005\ mol\ NaOH \\
n(HCl) = c . V = 0,02 . 0,1 = 0,002\ mol\ HCl \\
\Delta n = n(NaOH) – n(HCl) = 0,003\ mol$$
Koncentraci NaOH po reakci už spočítáme snadno:
$$c = \frac{n}{V} = \frac{0,003}{100 + 20} = 0,025\ M$$
Pro výpočet hodnoty pH nemusíme uvažovat vzniklý NaCl, protože jde o sůl silné kyseliny a zásady a hodnotu pH nám tedy neovlivní.
$$pOH = -\log c = -\log 0,025 = 1,60 \\
pH = 14 – pOH = 14 – 1,60 = 12,40$$
Výsledný roztok bude mít pH 12,40.
Skryj řešeníJaké pH bude mít roztok, který připravíme smísením 25 cm3 roztoku Ba(OH)2 o koncentraci 0,038 M s 50 cm3 roztoku HCl o pH 2,3? Objemové změny zanedbejte.
Ukaž řešeníNejprve musíme vytvořit rovnici neutralizační reakce:
Ba(OH)2 + 2 HCl → BaCl2 + 2 H2O
Z rovnice vidíme, že reaguje jeden mol hydroxidu s dvěma moly HCl. Hydroxid barnatý je silný hydroxid, který zcela disociuje i do druhého stupně, tzn. disociací jednoho molu hydroxidu vzniknou dva moly OH–:
Ba(OH)2 → Ba2+ + 2 OH–
Pro zjednodušení můžeme k výpočtu využít obecnou rovnici neutralizace:
H+ + OH– → H2O
Látkové množství OH– vypočítáme snadno, pomocí součinu objemu a koncentrace hydroxidu a vše násobíme dvěma:
$$n(OH^-) = c . V . 2 = 0,025 . 0,038 . 2 = 0,0019\ \textrm{mol OH}^-$$
Látkové množství H+ zjistíme z hodnoty pH kyseliny chlorovodíkové:
$$c(H^+) = 10^{-pH} = 10^{-2,3} = 0,0050\ M \\
n(H^+) = c . V = 0,0050 . 0,050 = 0,00025\ \textrm{mol H}^+$$
Vidíme, že OH– iontů je více, proto bude výsledné pH v zásadité oblasti. Nejprve musíme spočítat, kolik nám zůstane nezreagovaných OH– iontů:
$$n = 0,0019 – 0,00025 = 0,0016\ \textrm{mol OH}^-$$
K výpočtu pH pak už potřebujeme jen koncentraci OH-, nesmíme zapomenout na to, že objem výsledného roztoku se rovná součtu objemů původních roztoků (toto je zjednodušení, pokud bychom chtěli počítat přesně, museli bychom znát hustoty jednotlivých roztoků).
$$c = \frac{n}{V} = \frac{0,0016}{0,075} = 0,022 M \\
pOH = -\log c = -\log 0,022 = 1,66 \\
pH = 14 – pH = 12,34$$
Výsledné pH bude 12,34.
Skryj řešení100 cm3 roztoku kyseliny sírové o hodnotě pH 2,5 bylo zředěno vodou na celkový objem 250 cm3. Vypočítejte, jak se změnila hodnota pH.
Ukaž řešeníKyselina sírová je dvojsytná a do obou stupňů disociuje zcela, tzn. že můžeme popsat disociaci následující rovnicí:
H2SO4 → 2 H+ + SO42-
Koncentrace iontů H+ bude tedy dvojnásobná oproti koncentraci kyseliny.
pH = 2,5
c(H+) = 10-2,5 = 3,16.10-3 M
c(H2SO4) = 1,58.10-3 M
Pokud známe koncentraci kyseliny, můžeme snadno vypočítat její látkové množství a to použít pro výpočet koncentrace po zředění:
n = c . V = 1,58.10-3 . 0,1 = 1,58.10-4 mol H2SO4
\(\textrm{c}_2\ =\ \frac{\textrm{n}}{\textrm{V}}\ =\ \frac{1,58.10^{-4}}{0,25}\ =\ 6,33.10^{-4}\)
c(H+) = c2 . 2 = 6,33.10-4 . 2 = 1,26.10-3 M
pH = -log(c(H+)) = -log(1,26.10-3) = 2,89
Po zředění bude hodnota pH roztoku rovna 2,89.
Skryj řešeníNa jaký objem musíme zředit 25 cm3 roztoku o pH = 2,15, aby se hodnota pH změnila na 3,25?
Ukaž řešeníNejprve musíme vypočítat koncentraci výchozího roztoku:
$$\textrm{c = }10^{-\textrm{pH}}\ =\ 10^{-2,15}\ =\ 7,079.10^{-3}\textrm{ M}$$
Následně vypočítáme látkové množství HCl v roztoku:
$$\textrm{n = c . V = } 7,079.10^{-3}\ .\ 0,025\ =\ 1,770.10^{-4}\textrm{ mol HCl}$$
Během ředění se látkové množství nezmění, spočítáme si tedy výslednou koncentraci:
$$\textrm{c = }10^{-\textrm{pH}}\ =\ 10^{-3,25}\ =\ 5,623.10^{-4}\textrm{ M}$$
a nakonec objem konečného roztoku:
$$\textrm{V = }\frac{\textrm{n}}{\textrm{c}}\ =\ \frac{1,770.10^{-4}}{5,623.10^{-4}}\ =\ 0,315\ \textrm{dm}^3$$
Roztok musíme zředit na objem 315 cm3.
Skryj řešeníVypočítejte pH roztoku, který vznikne smísením 100 cm3 kyseliny octové o koncentraci 1 M s 50 cm3 roztoku NaOH o koncentraci 0,5 M. Pro jednoduchost neuvažujme objemové změny při mísení roztoků.
Ukaž řešeníPři smísení roztoků dojde k reakci mezi hydroxidem a kyselinou a vznikne octan sodný. Pro výpočet musíme nejprve zjistit látková množství:
n(CH3COOH) = c . V = 1 . 0,1 = 0,1 mol CH3COOH
n(NaOH) = c . V = 0,5 . 0,05 = 0,025 mol NaOH
Vidíme, že je kyselina v nadbytku. Po reakci tedy v roztoku zůstane 0,075 mol kyseliny octové a 0,025 mol octanu sodného. Tím jsme získali pufr a pro výpočet jeho pH použijeme Hendersonovu-Haaselbachovu rovnice:
$$\textrm{pH = pK}_\textrm{A}\ +\ \log\frac{[\textrm{A}^-]}{[\textrm{HA}]}$$
Koncentrace vypočítáme snadno, jako podíl látkového množství a objemu roztoku (150 cm3), pak je můžeme dosadit do rovnice výše:
$$\textrm{pH = pK}_\textrm{A}\ +\ \log\frac{[\textrm{A}^-]}{[\textrm{HA}]}\ =\ 4,76\ +\ \log\frac{0,17}{0,5}\ =\ 4,29$$
pH vzniklého roztoku bude 4,29.
Skryj řešeníVypočítejte objem roztoku kyseliny sírové o hodnotě pH 1,2, který obsahuje 0,050 mol kyseliny.
Ukaž řešeníNejprve musíme vypočítat molární koncentraci kyseliny sírové v roztoku, ta je poloviční oproti koncentraci iontů H+:
c(H+) = 10-pH = 10-1,2 = 0,0631 M
c(H2SO4) = c(H+) / 2 = 0,0631 / 2 = 0,0315 M
Teď už stačí jen dosadit do vztahu pro molární koncentraci:
$$\textrm{V = }\frac{\textrm{n}}{\textrm{c}}\ =\ \frac{0,050}{0,0315}\ =\ 1,585\ \textrm{dm}^3$$
1,585 dm3 roztoku kyseliny sírové o pH 1,2 obsahuje 0,050 mol kyseliny.
Skryj řešeníDalší kapitoly
- České chemické názvosloví
- Platné číslice a měření
- Základní chemické zákony
- Důležité veličiny a vztahy v chemii
- Výpočet stechiometrického vzorce
- Chemické rovnice a stechiometrické výpočty
- Koncentrace roztoků
- Rozpustnost, součin rozpustnosti
- Stavba atomu
- Periodická tabulka prvků a periodicita vlastností
- Chemická vazba
- VSEPR
- Komplexní sloučeniny
- Magnetické vlastnosti látek
- Termodynamika
- Chemická rovnováha
- Skupenské stavy látek
- Fázové rovnováhy
- Teorie kyselin a zásad
- pH, aktivita roztoku
- Elektrochemie
- Symetrie molekul
- Laboratorní technika
- Lineární regrese
- Jednotky tlaku
- Jednotky teploty
- Mohsova stupnice tvrdosti minerálů
- Odkazy
- Prezentace k semináři z obecné chemie