Bor je důležitý prvek, který lze připravit v několika alotropních formách. Mezi dobře charakterizované patří α-romboedrická, β-romboedrická a β-tetragonální modifikace.
α-romboedrický bor
Základní jednotkou je ikosaedr B12, kde je každý atom boru obklopen pěti sousedy. Ikosaedry jsou umístěny v mírně deformovaném nejtěsnějším uspořádání.
Protože má bor pouze tři valenční elektrony jsou vazby tvořeny dvouelektronovou třístředovou vazbou. V jednom ikosaedru je k dispozici 36 valenčních elektronů. Z nich je 26 využito v 13 molekulových orbitalech uvnitř ikosaedru a 6 elektronů vytváří šest kovalentních vazeb propojujících ikosaedry mezi sebou a zbylé čtyři elektrony jsou využity na šest dvouelektronových třístředových vazeb mezi ikosaedry.
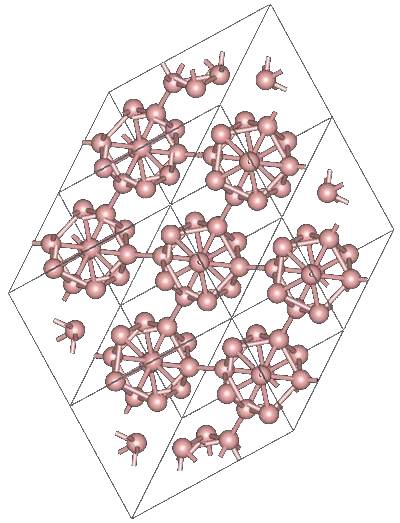
α-tetragonální bor
Čistou α-tetragonální modifikaci lze připravit pouze jako tenkou vrstvu na substrátu z karbidu (B50C2) nebo nitridu boru (B50N2).[2] V základní buňce obsahuje 50 atomů boru – 4 ikosaedry B12 a dva atomy boru, které je propojují.
β-romboedrický bor
Tato forma je termodynamicky nejstabilnější. Je tvořena středovým ikosaedrem, který je obklopen 12 jednotkami B7, ty okolo něj vytvářejí ikosaedr z ikosaedrů.
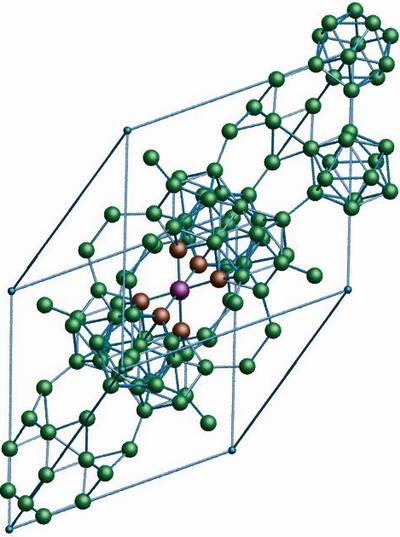
β-tetragonální bor
Má složitější strukturu než β-romboedrický bor. Poprvé byl připraven v roce 1960 redukcí BBr3 vodíkem na žhaveném vláknu (W nebo Re o průměru 0.025 mm) při teplotách 1270-1550 °C.[3]
γ-bor
Tato fáze byla poprvé publikována v roce 1965. γ-bor má strukturu typu NaCl, základní buňka je tvořena opět iokosaedry B12, ale v tomto případě jsou mezery mezi nimi vyplněny páry B2, které fungují jako protiionty.[4]
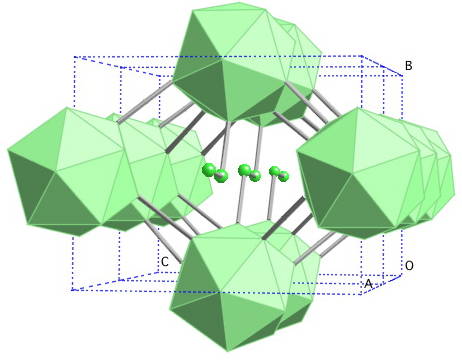
Supravodivost za vysokého tlaku
Za zvýšeného tlaku vykazují některé alotropické modifikace boru supravodivost.[5]
Literatura
- Allotropes of boron
- GREENWOOD, N. N. a Alan EARNSHAW. Chemie prvků. Praha: Informatorium, 1993. ISBN 80-85427-38-9. s.176-178
- A new polymorph of boron
- Ionic high-pressure form of elemental boron
- Superconductivity in Boron