Samarium, Sm, je pátý lanthanoid. Je to středně tvrdý, stříbrný kov. Využívá se hlavně pro přípravu silných permanentních magnetů a speciálních skel a keramiky. Ve sklářství se přídavků samaria využívá ke zvýšení absorpce infračerveného záření.
| Atomové číslo | 62 | Počet stabilních izotopů | 3 |
| Atomová hmotnost | 150,36 | Elektronová konfigurace | [Xe] 4f6 6s2 |
| Teplota tání [°C] | 1072 | Teplota varu [°C] | 1900 |
| Elektronegativita | 1,17 | Hustota [g.cm-3] | 7,52 |
Výskyt
V zemské kůře je jeho koncentrace asi 6 mg/kg. Vyskytuje se v minerálech společně s ostatními lanthanoidy.

Izotopy
Samarium má celkem pět stabilních izotopů – 144Sm, 149Sm (pravděpodobně podléhá α rozpadu, poločas je ale větší než 2×1015 let), 150Sm, 152Sm a 154Sm.[6]
| Izotop | Poločas rozpadu | Zastoupení v přírodě [%] |
| 144Sm | stabilní | 3,08 |
| 145Sm | 340 dne | umělý |
| 146Sm | 6,8×107 let | umělý |
| 147Sm | 1,06×1011 let | 15,00 |
| 148Sm | 7×1015 | 11,25 |
| 149Sm | stabilní | 13,82 |
| 150Sm | stabilní | 7,37 |
| 151Sm | 88,8 let | umělý |
| 152Sm | stabilní | 26,74 |
| 153Sm | 46,28 hodin | umělý |
| 154Sm | stabilní | 22,74 |
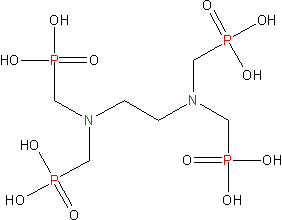
Izotop 147Sm se využívá v jaderné geochronologii. Komplex izotopu 153 s ligandem EDTMP nachází důležité využití v nukleární medicíně při tišení bolestí.[3]
Chemické vlastnosti
Nejběžnější oxidační číslo Sm ve sloučeninách je III, setkáváme se i se sloučeninami, kde je jeho oxidační číslo II. Nejstabilnějším oxidem je Sm2O3, lze jej za vysoké teploty (1000 °C) redukovat kovovým samariem na SmO. Reaguje se všemi halogeny za vzniku SmX3, které lze opět redukovat samariem, lithiem nebo sodíkem na SmX2. Ve vodným roztocích vytváří komplexní ionty, ve kterých je samarium obklopeno devíti molekulami vody.[4]
S vodou reaguje za vzniku hydroxidu a uvolnění vodíku:
2 Sm + 6 H2O → 2 Sm(OH)3 + 3 H2
Na vzduchu se pomalu pokrývá vrstvou oxidu a hoří přímo za vzniku Sm2O3:
4 Sm + 3 O2 → 2 Sm2O3
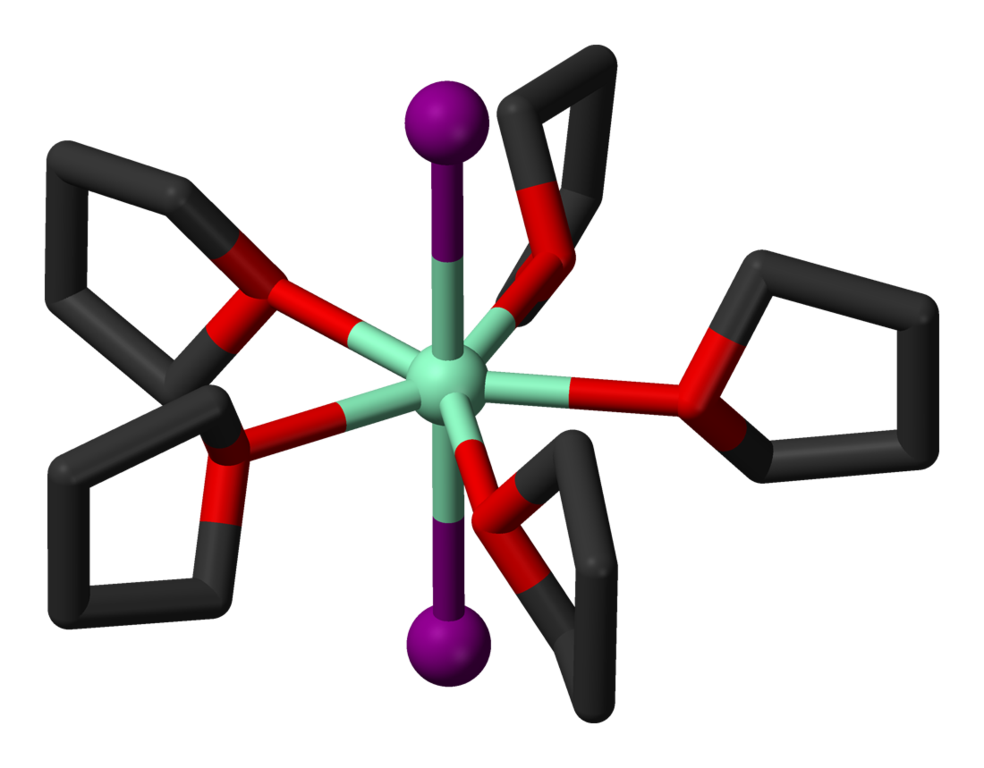
Jodid samarnatý
Jodid samarnatý je zelená pevná látka, v organické syntéza známá jako Kaganovo činidlo. Využívá se jako silné redukční činidlo. Připravuje se reakcí kovového samaria s dijodmethanem nebo 1,2-dijodethanem.
Samarium-kobaltové magnety
Jednou z hlavních aplikací samaria je výroba velmi silných permanentních magnetů, silnějších než jsou neodymové magnety. Jde o slitiny s kobaltem, základní komerčně dostupné typy magnetů mají složení SmCo5 a Sm2Co17.[7] Na rozdíl od neodymových magnetů zvládnou fungovat při výrazně vyšších teplotách, což je důležité např. v armádních aplikacích.[8]
NMR
Samarium má dva NMR aktivní izotopy, oba mají spin 7/2 a nízkou citlivost.
| 147Sm | 149Sm | |
| Spin | 7/2 | 7/2 |
| Zastoupení v přírodě [%] | 15,0 | 13,8 |
| Rezonanční frekvence v poli 1 T | 1,7748 | 1,4631 |
| Jaderný magnetický moment | -0,8149 | -0,6718 |
| Citlivost vůči 1H | 0,00152 | 0,00085 |
Odkazy
- Samarium na české wikipedii
- Samarium na anglické wikipedii
- HÁLA, Jiří. Radioaktivní izotopy. Tišnov: Sursum, 2013, 374 s. ISBN 978-80-7323-248-1.
- The geometry of the nonaaqualanthanoid(3+) complex in the solid bromates and ethyl sulphates
- Samarium(II) iodide
- Discovery of samarium, europium, gadolinium, and terbium isotopes
- Everything You Need to Know About Samarium Cobalt Magnets
- USA doplácejí na celní válku. I tomahawkům chybí samarium z Číny
Navigace
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 |
| H | He | ||||||||||||||||
| Li | Be | B | C | N | O | F | Ne | ||||||||||
| Na | Mg | Al | Si | P | S | Cl | Ar | ||||||||||
| K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr |
| Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe |
| Cs | Ba | La | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn |
| Fr | Ra | Ac | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og |
| Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu |
| Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr |