Merkurimetrické titrace využívají jako odměrné činidlo roztok dusičnanu rtuťnatého. Používají se hlavně ke stanovení halogenidů, jde o levnější alternativu k argentometrii. Nevýhodou je samozřejmě práce s toxickými sloučeninami rtuti.
Merkurimetrie patří mezi komplexometrické titrace, tyto jsou založeny na tvorbě nedisociovaných, rozpustných komplexů.
Příprava odměrného roztoku
Navážku dusičnanu rtuťnatého, Hg(NO3)2, rozpustíme v odměrné baňce, po kapkách přidáváme koncentrovanou kyselinu dusičnou, až do vyčeření roztoku a poté doplníme baňku vodou po rysku.
Přesnou koncentraci stanovíme titrací roztoku NaCl na indikátor difenylkarbazid.
Indikátor
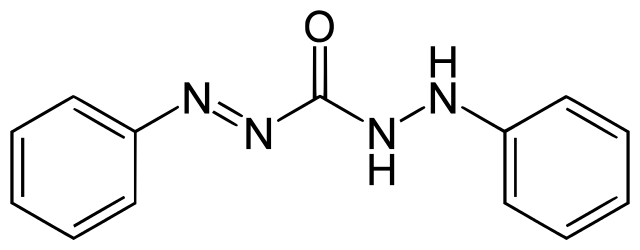
Jako indikátor se nejčastěji využívá difenylkarbazid, buď samotný nebo ve směsi s difenylkarazidem nebo thiokyanatanem železitým, Fe(SCN)3. Titrujeme do vzniku fialově-modrého zabarvení rtuťnatého chelátu.
Druhým možným indikátorem je nitroprussid sodný, Na2[Fe(CN)5NO], jde o stanovení dle Votočka. Využívá se hlavně při titracích Cl– a CN–.

Stanovení
Při stanovení chloridů probíhá reakce, kterou můžeme popsat takto:
4 NaCl + Hg(NO3)2 → Na2[HgCl4] + 2 NaNO3
Dochází ovšem k následnému rozpadu komplexů:
HgCl42- → HgCl3– → HgCl2 → HgCl+
Poměr Cl:Hg je tedy 1:1.
Odkazy
Další kapitoly
- České chemické názvosloví
- Platné číslice a měření
- Základní chemické zákony
- Důležité veličiny a vztahy v chemii
- Výpočet stechiometrického vzorce
- Chemické rovnice a stechiometrické výpočty
- Koncentrace roztoků
- Rozpustnost, součin rozpustnosti
- Stavba atomu
- Periodická tabulka prvků a periodicita vlastností
- Chemická vazba
- VSEPR
- Komplexní sloučeniny
- Magnetické vlastnosti látek
- Termodynamika
- Chemická rovnováha
- Skupenské stavy látek
- Fázové rovnováhy
- Teorie kyselin a zásad
- pH, aktivita roztoku
- Elektrochemie
- Symetrie molekul
- Laboratorní technika
- Lineární regrese
- Jednotky tlaku
- Jednotky teploty
- Mohsova stupnice tvrdosti minerálů
- Odkazy
- Prezentace k semináři z obecné chemie