Aromatické sloučeniny uhlíku jsou velmi dobře známé, ale jak to vypadá u těžších prvků této skupiny? Nedávno byl zveřejněn teoretický článek týkající se stability germabenzenů, což mě přivedlo na myšlenku sepsat trochu delší článek o vybraných aromatických sloučeninách prvků 14. skupiny. Samozřejmě nepůjde o kompletní výpis, ale pro zájem je zde seznam použité literatury, kde najdou více informací.
14. skupina obsahuje prvky uhlík, křemík, germanium, cín, olovo a flerovium. V tomto článku vynecháme flerovium, protože informací o chemii tohoto prvku je velmi málo a samozřejmě velice silně osekám informace o aromatických sloučeninách uhlíku, protože těch je naopak extrémně moc a je jim věnována spousta jiných informačních zdrojů.
Aromatické sloučeniny
Aromatické sloučeniny jsou cyklické molekuly s konjugovaným systémem násobných vazeb, které vykazují vysokou stabilitu a poměrně nízkou reaktivitu. Aromatické látky musí splňovat tři podmínky:[1]
- Molekula musí být planární (rovinná)
- Molekula musí obsahovat konjugovaný systém násobných vazeb, tzn. musí se pravidelně střídat jednoduchá a dvojná vazba
- Počet π elektronů musí odpovídat výrazu 4n+2 (Hückelovo pravidlo), kde n ≥ 0
Uhlík
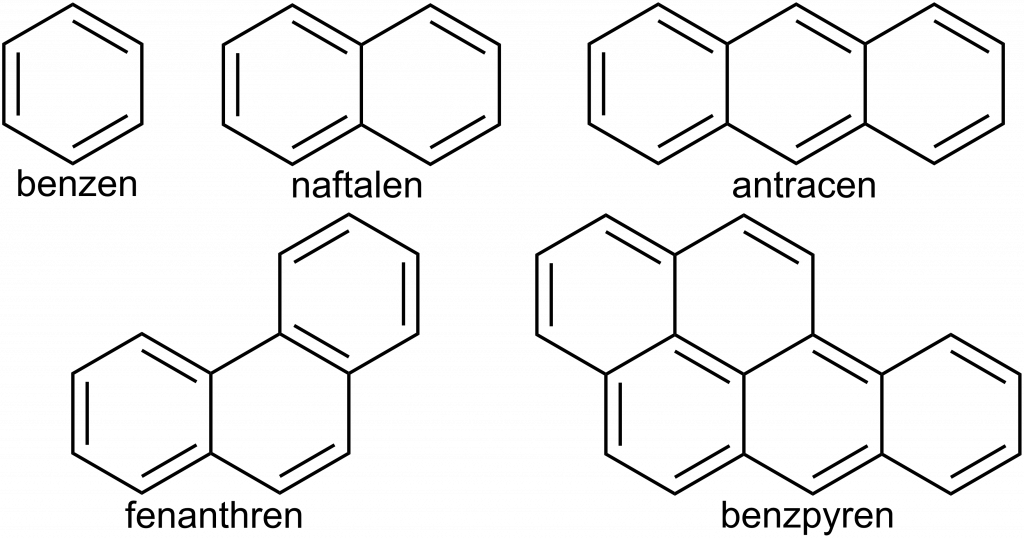
Asi nejznámějším příkladem je benzen, tzn. cyklická šestičlenná molekula s 6 π elektrony (4×1 + 2).
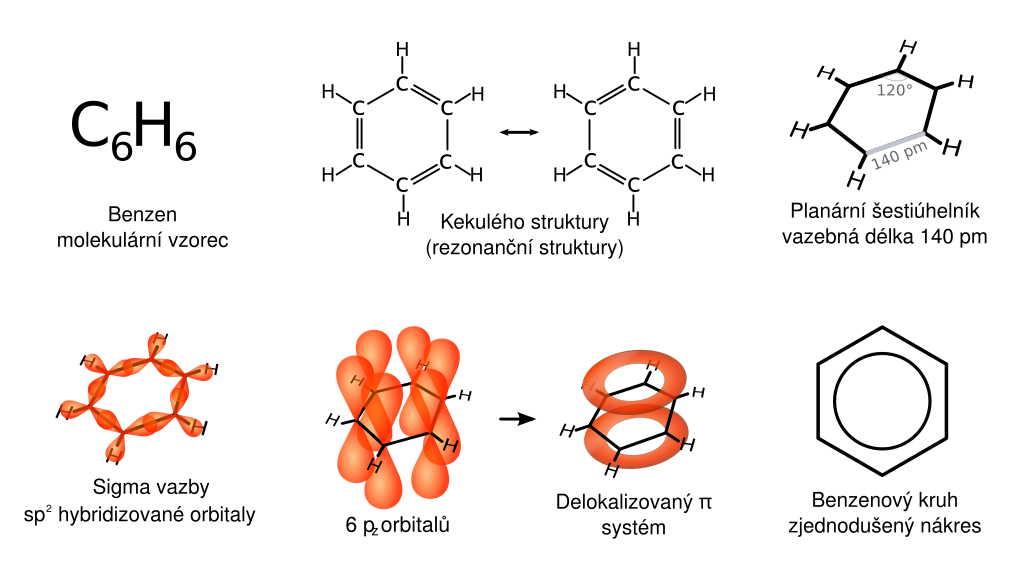
Benzen není samozřejmě jedinou aromatickou sloučeninou, v dnešní době jich známe obrovské množství (viz obrázek dole).
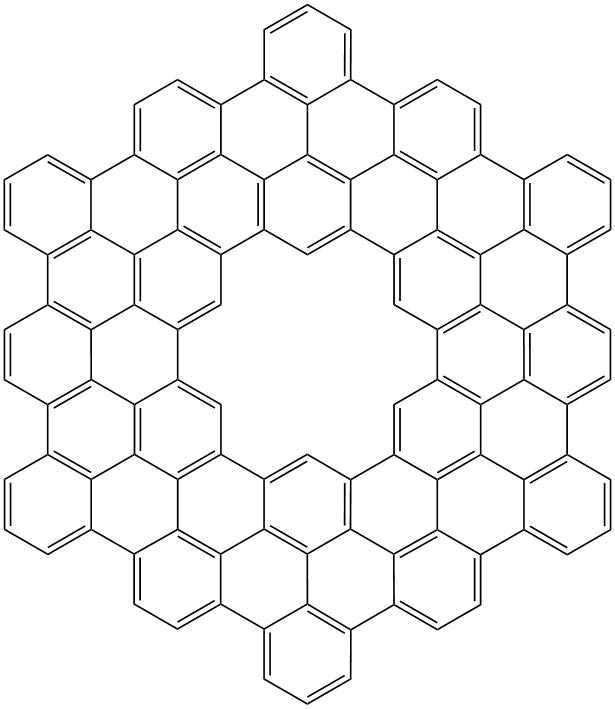
V roce 2020 byla publikována příprava cykloarenu se 108 atomy uhlíku.
Křemík
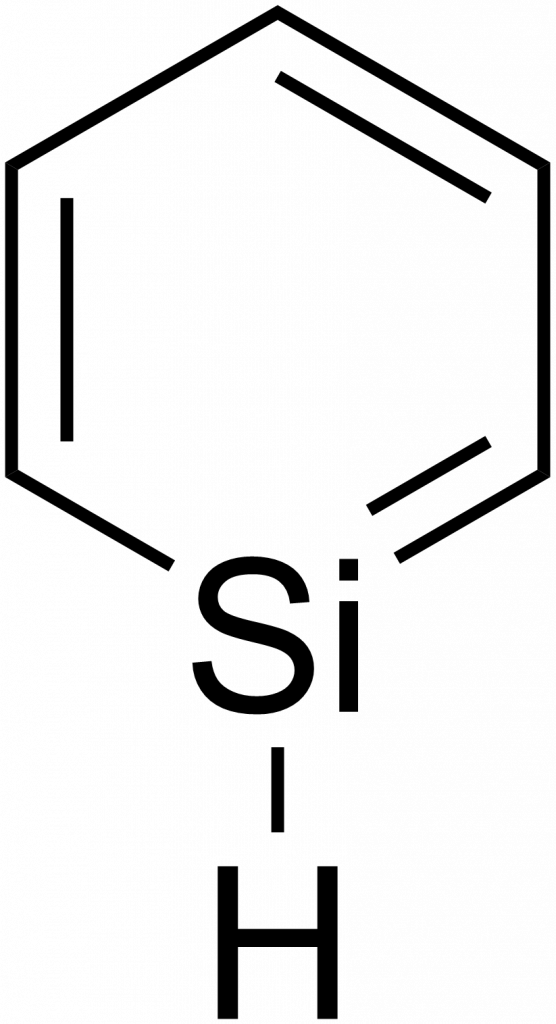
Křemík je v mnohém podobný uhlíku, ale také se od uhlíku značně odlišuje. Pokud v benzenu nahradíme jeden uhlík křemíkem, získáme silabenzen, C5H6Si. Nestabilní sloučeninu, kterou lze studovat pouze v matrici za velmi nízkých teplot, ale známe několik jeho více či méně stabilních derivátů.
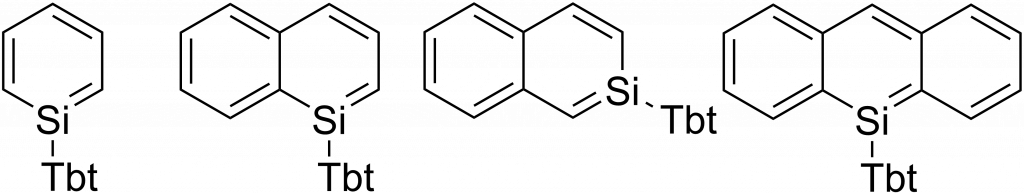
Stabilitu lze zvýšit nahrazením protonu na křemíku za stericky náročnější skupinu, např. Tbt skupinu (2,4,6-tris[bis(trimethylsilyl)methyl]fenyl)).
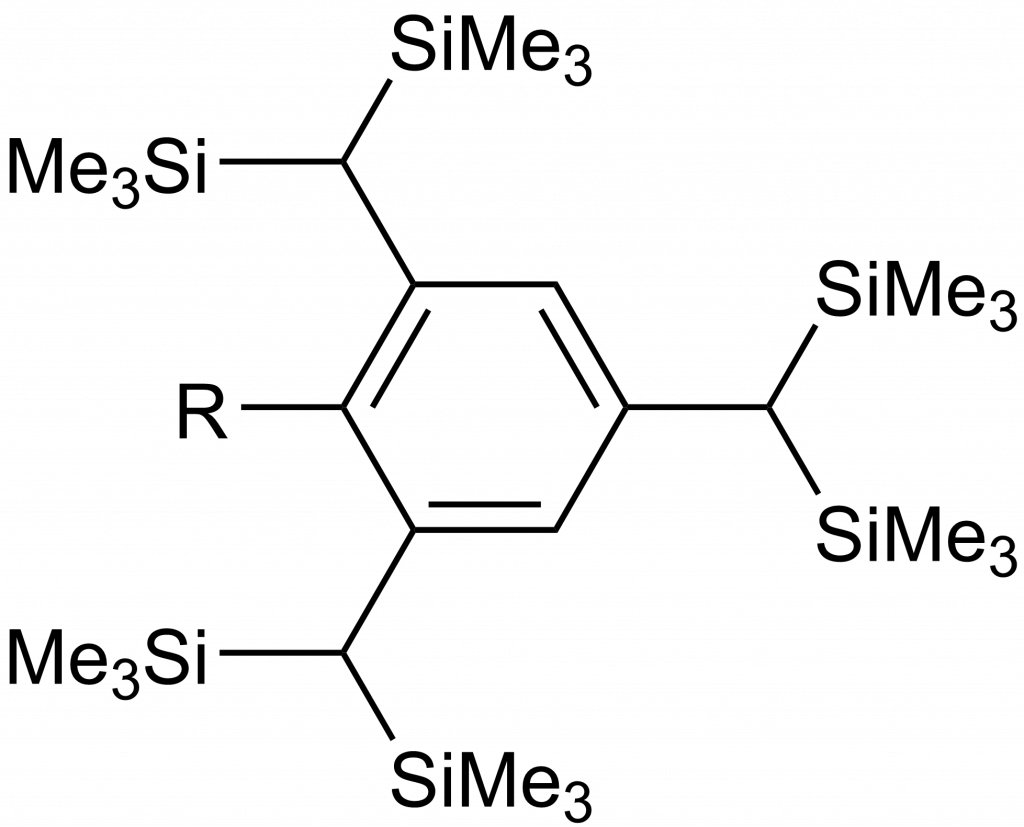
Díky této skupině se podařilo připravit a charakterizovat celou řadu aromatických sloučenin křemíku, viz obrázek dole. U těchto sloučenin byla také prokázána delokalizace elektronů a existence planárního cyklického systému.[2]
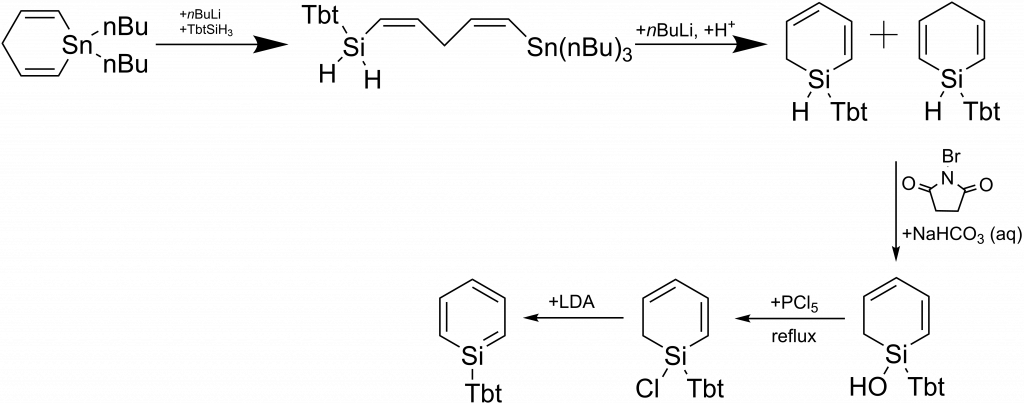
Syntéza silabenzenu vycházela ze stannacyklohexa-2,5-dienu, který reagoval s butyllithiem a následně s derivátem silanu TbtSiH3. Získaný produkt byl zacyklen reakcí s butyllithiem. Následně byl vodík vázaný na křemík postupně substituován, až na konečný chlorid. Ten byl redukován pomocí diisopropylamidu lithného (LDA, lithium diisopropylamide) za vzniku derivátu silabenzenu.
Germanium
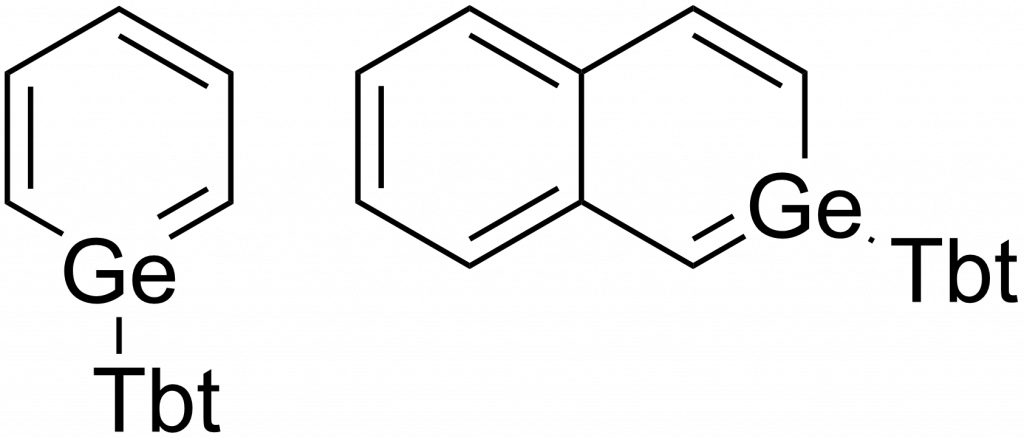
U germania známe analogy benzenu a naftalenu, podobně jako u křemíku, opět se využívá stabilizace pomocí skupiny Tbt.[2]
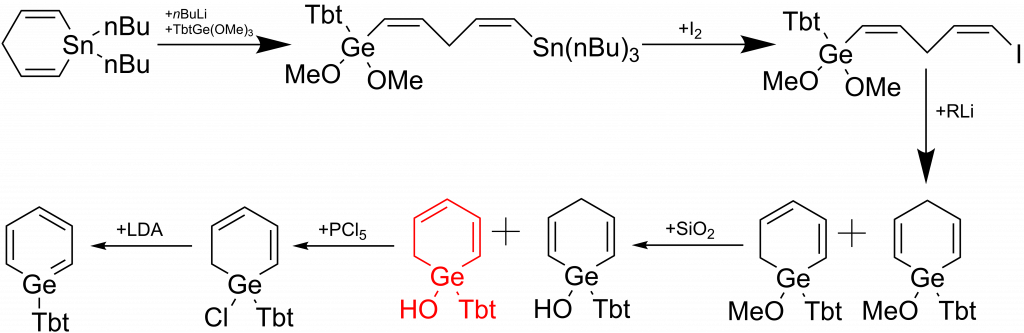
První příprava stabilního derivátu germabenzenu byla publikována v roce 2002. Syntéza byla velice podobná popsané syntéza u silabenzenu. Vycházela opět ze stannacyklohexa-2,5-dienu, který reagoval s butyllithiem a následně s TbtGe(OMe)3. Cín byl poté zaměněn za jodid, reakcí s elementárním jódem a produkt byl zacyklen pomocí butyllithia. Následně docházel k substituci skupin na germaniu, až na konečný chlorid. Ten byl nakonec redukován pomocí diisopropylamidu lithného (LDA, lithium diisopropylamide) za vzniku substituovaného germabenzenu.
Příprava těchto sloučenin je poměrně náročná, proto jsou studovány i pomocí výpočetních metod (ty jsou zpravidla levnější než syntéza). Nově publikovaný článek se zabývá hypotetickými molekulami odvozenými od benzenu a obsahujícími 1-6 atomů germania.[3]
Cín
Samotný stannabenzen (C5H6Sn) nebyl dosud izolován a je studován pouze teoreticky.[4] Známe, ale několik jeho derivátů. V roce 2010 byla publikována příprava derivátu s TBT ligandem, který je ale nestabilní a za laboratorní teploty vytváří dimer.[5]

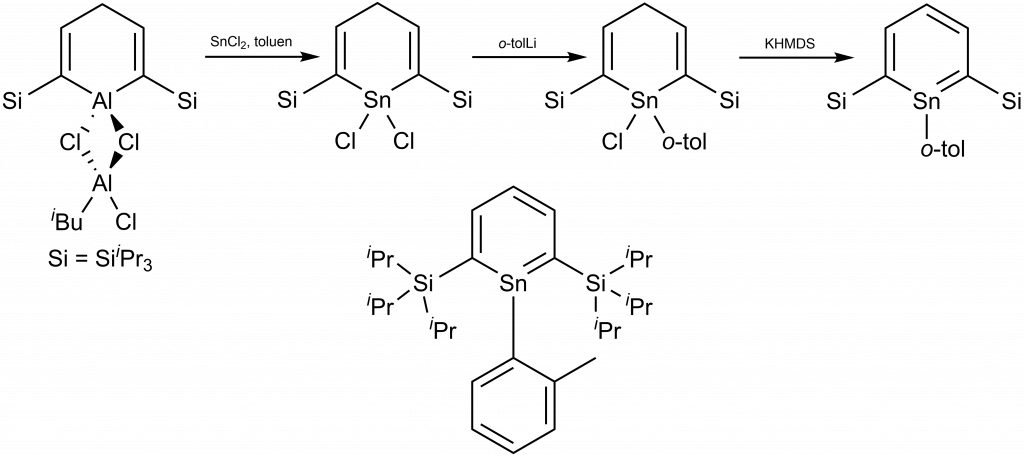
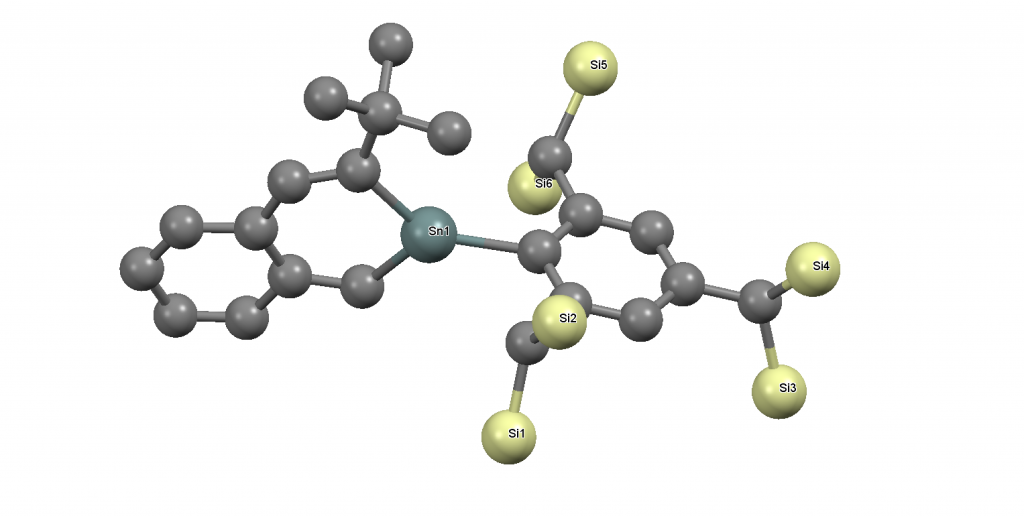
V roce 2019 byla publikována příprava stabilního derivátu stannabenzenu, u něhož nebyla pozorována dimerace ani za zvýšené teploty.[6]
Reakce vycházela z aluminacyklohexadienu, kde byl reakcí s chloridem cínatým (SnCl2) zaměněn hliník za cín. Reakcí s ortho-tolyllithiem byla na cín zavedena o-tol skupina. Posledním krokem byla reakce s bis(trimethylsilyl)amidem draselným (KHMDS, KN(SiMe3)2), kdy došlo k odštěpení posledního chloridu a vytvoření aromatického systému.
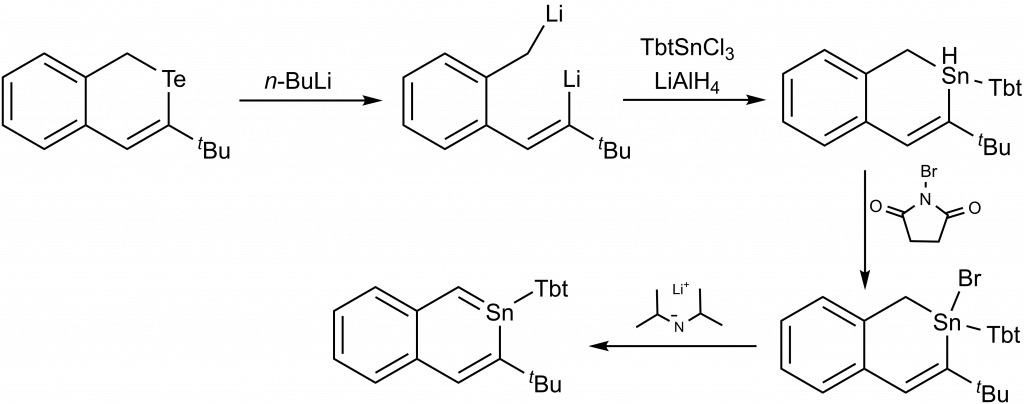
V roce 2005 byla publikována příprava derivátu naftalenu s jedním atomem cínu (2-stannanaftalenu).[6]
Příprava vycházela z isotellurochromenu, reakcí s dvěma ekvivalenty n-butyllithia došlo k otevření kruhu. Následující reakcí s TbtSnCl3 a redukcí pomocí tetrahydridohlinitanu došlo k obnovení cyklu. Pomocí N-bromsukcinimidu byl na cín navázán brom a v dalším kroku byl tento produkt redukován pomocí diisopropylamidu lithného. Pomocí NMR a RTG bylo prokázáno, že substituovaný naftalen má stále aromatický charakter.
Olovo
Review z roku 2004 uvádí, že plumababenzen (ale ani stannabenzen) nebyl dosud připraven, ani pozorován.[2] Zkoušel jsem (srpen 2025) prohledávat WOS, ale bez úspěchu, takže situace se pravděpodobně zatím nezměnila.
Závěr
Nejde samozřejmě o vyčerpávající výčet aromatických sloučenin prvků 14. skupiny PSP, ale snažil jsem tady vypíchnout ty (alespoň z mého pohledu) zajímavější informace. Článek se bude pravděpodobně v čase měnit a doufejme i rozšiřovat.
Odkazy
- Hückel’s Rule
- New Progress in the Chemistry of Stable Metallaaromatic Compounds of Heavier Group 14 Elements
- Structure and Aromaticity of Germabenzenes: A Computational Investigation
- Topological characteristics of the Ring Critical Points and the aromaticity of groups IIIA to VIA hetero-benzenes
- Generation of Stannabenzenes and Their Properties
- A Monomeric Stannabenzene: Synthesis, Structure, and Electronic Properties
- A Stable Neutral Stannaaromatic Compound: Synthesis, Structure and Complexation of a Kinetically Stabilized 2-Stannanaphthalene