Infračervená spektroskopie je metoda z oboru molekulové spektroskopie, která využívá interakci infračerveného záření se studovaným vzorkem. Infračervené záření je část elektromagnetického spektra zhruba ohraničená vlnovými délkami 700 nm – 1 mm, čili mezi viditelným a mikrovlnným zářením. Během experimentu dochází k absorpci infračerveného záření vzorkem. Získané pásové spektrum lze pak využít jak ke kvalitativní, tak i kvantitativní analýze vzorku. Lze měřit vzorky ve všech třech skupenstvích.
Dělení podle vlnové délky IR záření
| Vlnová délka [μm] | Vlnočet [cm-1] | Metoda |
| 0,8 – 2,5 | 14 000 – 4000 | NIR (IR spektroskopie v blízké oblasti) |
| 2,5 – 25 | 4000 – 400 | MIR (IR spektroskopie ve střední oblasti) |
| 25 – 1000 | 400 – 10 | FIR (IR spektroskopie ve vzdálené oblasti) |
Elektromagnetické záření
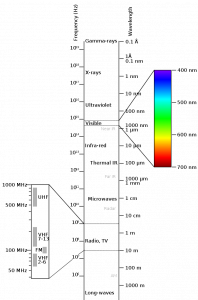
Infračervená spektroskopie studuje interakci elektromagnetického (infračerveného) záření se vzorkem. Elektromagnetické záření je příčné vlnění, má elektrickou a magnetickou složku, které jsou na sebe kolmé. Vzniká při pohybu nabité částice. Je charakterizováno energií, z jejíž hodnoty odvozujeme vlnovou délku, frekvenci a vlnočet. Ve vibrační spektroskopii se nejčastěji setkáváme s vlnočtem (vlnovým číslem), což je počet vln, připadajících na dráhu 1 cm ve směru šíření záření.
$$E = hf = \frac{hc}{\lambda} = hc\tilde{\nu}$$
Historie
Infračervené záření bylo objeveno roku 1800 astronomem Williamem Herschelem, při měření tepelného záření slunce. První studie interakce IR záření se vzorky byly provedeny až začátkem 20. století, v té době se totiž povedlo sestrojit použitelný detektor pro IR záření.
První prototyp IR spektrometru byl sestrojen ve 30. Letech a první komerční spektrometr ho brzy následoval. Až do 70. let byly spektrometry výhradně disperzní, jako monochromátor se využíval hranol nebo mřížka. Důležitým mezníkem bylo zavedení IR spektroskopie s Fourierovou transformací. Tyto spektrometry využívají Michaelsonův interferometr, který byl zkonstruován již roku 1891. Pro jejich zavedení do praxe bylo nutné spojení spektrometru s počítačem, jelikož tato metoda vyžaduje poměrně složité výpočty.
Vznik spekter
Infračervená spektra vznikají absorpcí záření vzorkem. Energie fotonů infračerveného záření (1-60 kJ/mol) nestačí na excitaci elektronů, ale je dostatečná pro změnu rotačního nebo vibračního stavu molekuly, tzn. ke změně amplitudy vibrace nebo rychlosti rotace molekuly.
Aby mohlo dojít k absorpci, musí během vibrace docházet ke změně dipólového momentu. Proto např. molekuly dusíku a kyslíku neposkytují žádné vibrační pásy. Jde o lineární molekuly tvořené stejnými atomy, proto mají nulový dipólový moment, při vibraci zůstává geometrie zachována a dipolmoment s nemění.
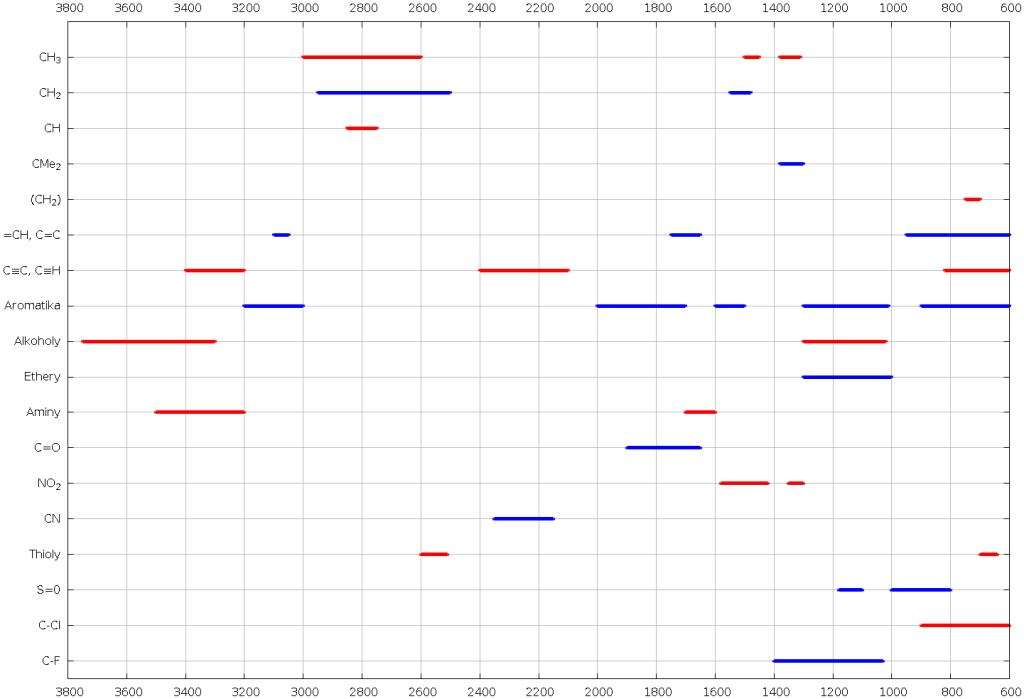
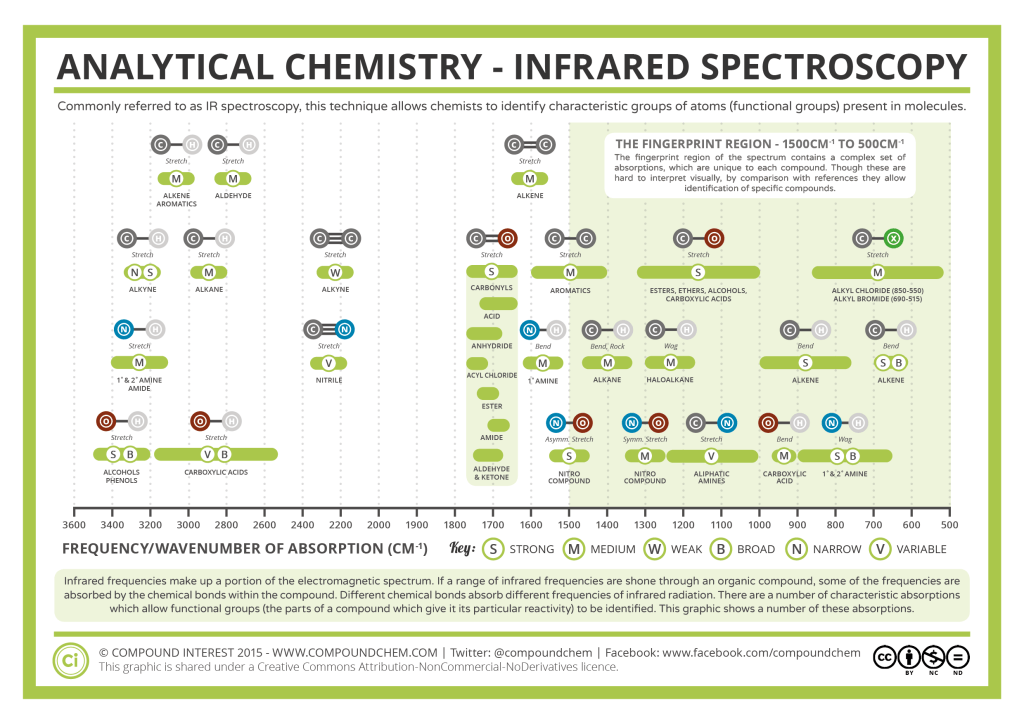
Charakteristické frekvence skupin
Tabulka s vibračními pásy vybraných skupin
Infračervená mikroskopie
Pro analýzu větších předmětů je výhodná infračervená mikroskopie. Mikroskop umožňuje přesné zacílení IR paprsku. Můžeme tak provádět analýzy defektů, rozložení složek v tabletě, apod. Pěkně zpracované video o FT-IR mikroskopii můžeme najít na youtube kanálu firmy Bruker.
Literatura
- Infračervená absorpční spektroskopie a detekce plynů
- Biomolecular and bioanalytical applications of infrared spectroscopy – A review
7 Replies to “Infračervená spektroskopie”