Uran, U, je slabě radioaktivní, stříbrnobílý kov, po delším stání na vzduchu šedne vlivem oxidace. Patří mezi aktinoidy. Jeho hustota je přes 19 g.cm-3, patří mezi nejtěžší prvky.
| Atomové číslo | 92 | Počet stabilních izotopů | 0 |
| Atomová hmotnost[8] | 238,029 | Elektronová konfigurace | [Rn] 5f3 6d1 7s2 |
| Teplota tání [°C] | 1132,3 | Teplota varu [°C] | 3818 |
| Elektronegativita | 1,38 | Hustota [g.cm-3] | 19,01 |
Hlavní využití nachází uran v jaderné energetice, jako palivo do reaktorů, příp. náplň do nukleárních zbraní. Pro tyto účely se uran zpravidla obohacuje, tzn. zvyšuje se koncentrace štěpitelného izotopu 235U.

Izotopy
Uran, stejně jako ostatní aktinoidy nemá žádný stabilní izotop. Přírodní uran se skládá ze dvou izotopů s dlouhým poločasem rozpadu – 235U (7,04×108 let, 0,720 %) a 238U (4,468×109 let, 99,274 %) a izotopu 234U (2,455×105 let, 0,005 %), který je jedním z meziproduktů rozpadové řady 238U.
| Izotop | Zastoupení [%] | Poločas rozpadu |
| 232U | syntetický | 68,9 let |
| 233U | stopové | 1,592×105 let |
| 234U | 0,005 | 2,455×105 let |
| 235U | 0,720 | 7,04×109 let |
| 236U | stopové | 2,342×107 let |
| 238U | 99,274 | 4,468×109 let |
V roce 2021 byla publikována příprava nejlehčího známého izotopu 214U:[7]
$$^{182}_{\ \ 74}\textrm{W}\ +\ ^{36}_{18}\textrm{Ar}\ \rightarrow\ ^{214}_{\ \ 92}\textrm{U}\ +\ 4\ ^{1}_{0}\textrm{n}$$
Chemické vlastnosti
Uran vytváří sloučeniny v oxidačních číslech +III až +VI, nejčastěji vystupuje ve formě iontů: U3+, U4+, UVO2+ a UVIO22+.

U2@C60
Velice zajímavou (zatím ale jen hypotetickou) sloučeninou uranu je endohedrální derivát fullerenu C60, který uvnitř klece obsahuje dva atomy uranu vázané do kationtu [U2]6+. Tato látka zatím nebyla připravena, ale byla studována pomocí DFT výpočtů. Ty ukázaly že sloučenina bude stabilní a její strukturu bude možná popsat vzorcem U26+@C606-.[9]
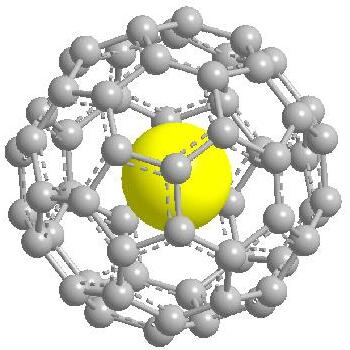
Zajímavé jsou i vazebné poměry v iontu [U2]6+, výpočty prokázaly, že vazba bude tvořená šesti jednoelektronovými dvoustředovými vazbami.
NMR
Uran má jeden NMR aktivní izotop s velice nízkou citlivostí. Je kvadrupolární a poskytuje signály s velkou pološířkou.
| 235U | |
| Spin | 7/2 |
| Zastoupení v přírodě [%] | 0,7204 |
| Citlivost vzhledem k 1H | 1,11×10-6 |
| Citlivost vzhledem k 13C | 6,53×10-3 |
| Rezonanční frekvence v poli 1 T | 0,83 |
| Jaderný magnetický moment | -0,83 |
Odkazy
- Uran na české wikipedii
- Uran na anglické wikipedii
- Nitrite complexes of uranium and thorium
- Získávání uranu z mořské vody
- Uranium extraction: Coordination chemistry in the ocean
- 235U NMR
- New α-Emitting Isotope 214U and Abnormal Enhancement of α-Particle Clustering in Lightest Uranium Isotopes
- Atomic Weight of Uranium
- Dimetalloendofullerene U2@C60 Has a U−U Multiple Bond Consisting of Sixfold One-Electron-Two-Center Bonds
Navigace
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 |
| H | He | ||||||||||||||||
| Li | Be | B | C | N | O | F | Ne | ||||||||||
| Na | Mg | Al | Si | P | S | Cl | Ar | ||||||||||
| K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr |
| Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe |
| Cs | Ba | La | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn |
| Fr | Ra | Ac | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og |
| Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu |
| Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr |
8 Replies to “Uran”